 Что такое химия?
Что такое химия?
ХИМИЯ (возможно, от греч. Chemia — Хемия, одно из древнейших названий Египта), наука, изучающая превращения веществ, сопровождающиеся изменением их состава и (или) строения. Химические процессы (получение металлов из руд, крашение тканей, выделка кожи и др.) использовались человечеством уже на заре его культурной жизни. В 3-4 вв. зародилась алхимия, задачей которой было превращение неблагородных металлов в благородные. С эпохи Возрождения химические исследования все в большей степени стали использовать для практических целей (металлургия, стеклоделие, производство керамики, красок); возникло также особое медицинское направление алхимии — ятрохимия. Во 2-й пол. 17 в. Р. Бойль дал первое научное определение понятия «химический элемент». Период превращения химии в подлинную науку завершился во 2-й пол. 18 в., когда был сформулирован сохранения массы закон при химических реакциях (см. также М. В. Ломоносов, А. Лавуазье). В нач. 19 в. Дж. Дальтон заложил основы химической атомистики, А. Авогардо ввел понятие «молекула». Эти атомно-молекулярные представления утвердились лишь в 60-х гг. 19 в. Тогда же А. М. Бутлеров создал теорию строения химических соединений, а Д. И. Менделеев открыл периодический закон (см. Периодическая система элементов Менделеева). С кон. 19 — нач. 20 вв. важнейшим направлением химии стало изучение закономерностей химических процессов.
В современной химии отдельные ее области — неорганическая химия, органическая химия, физическая химия, аналитическая химия, химия полимеров стали в значительной степени самостоятельными науками. На стыке химии и других областей знания возникли, напр., биохимия, агрохимия, геохимия. На законах химии базируются такие технические науки, как химическая технология, металлургия.
В современной химии отдельные ее области — неорганическая химия, органическая химия, физическая химия, аналитическая химия, химия полимеров стали в значительной степени самостоятельными науками. На стыке химии и других областей знания возникли, напр., биохимия, агрохимия, геохимия. На законах химии базируются такие технические науки, как химическая технология, металлургия.

 Д.М. Менделеев
Д.М. Менделеев

МЕНДЕЛЕЕВ Дмитрий Иванович (1834-1907), русский химик, выдающийся, разносторонний ученый, педагог.
Открыл (1869) периодический закон химических элементов — один из основных законов естествознания. Оставил св. 500 печатных трудов, среди которых классические «Основы химии» (ч. 1-2, 1869-71, 13 изд., 1947) — первое стройное изложение неорганической химии. Автор фундаментальных исследований по химии, химической технологии, физике, метрологии, воздухоплаванию, метеорологии, сельскому хозяйству, экономике, народному просвещению и др., тесно связанных с потребностями развития производительных сил России. Заложил основы теории растворов, предложил промышленный способ фракционного разделения нефти, изобрел вид бездымного пороха, пропагандировал использование минеральных удобрений, орошение засушливых земель. Один из инициаторов создания Русского химического общества (1868). Профессор Петербургского университета (1865-90), ушел в отставку в знак протеста против притеснения студенчества. С 1876 член-корреспондент Петербургской АН, в 1880 выдвигался в академики, но был забаллотирован, что вызвало резкий общественный протест. Организатор и первый директор (1893) Главной палаты мер и весов (ныне ВНИИ метрологии им. Менделеева).
Открыл (1869) периодический закон химических элементов — один из основных законов естествознания. Оставил св. 500 печатных трудов, среди которых классические «Основы химии» (ч. 1-2, 1869-71, 13 изд., 1947) — первое стройное изложение неорганической химии. Автор фундаментальных исследований по химии, химической технологии, физике, метрологии, воздухоплаванию, метеорологии, сельскому хозяйству, экономике, народному просвещению и др., тесно связанных с потребностями развития производительных сил России. Заложил основы теории растворов, предложил промышленный способ фракционного разделения нефти, изобрел вид бездымного пороха, пропагандировал использование минеральных удобрений, орошение засушливых земель. Один из инициаторов создания Русского химического общества (1868). Профессор Петербургского университета (1865-90), ушел в отставку в знак протеста против притеснения студенчества. С 1876 член-корреспондент Петербургской АН, в 1880 выдвигался в академики, но был забаллотирован, что вызвало резкий общественный протест. Организатор и первый директор (1893) Главной палаты мер и весов (ныне ВНИИ метрологии им. Менделеева).


 Разделы химии
Разделы химии
ОРГАНИЧЕСКАЯ ХИМИЯ, изучает соединения углерода с другими элементами — т. н. органические соединения и законы их превращений. Как самостоятельная область химии стала складываться лишь в 19 в.; термин «органическая химия» введен Й. Берцелиусом в 1827. Большое влияние на развитие органической химии оказала теория химического строения (А. М. Бутлеров, 1861). Способность углерода соединяться с большинством элементов и образовывать молекулы самого различного состава и строения (цепного, циклического, с простыми и кратными связями между атомами) обусловливает огромное многообразие органических соединений (к 90-м гг. 20 в. их число превысило 10 млн.). Синтез многочисленных органических веществ привел к созданию новых отраслей промышленности — синтетических красителей, полимеров, искусственного жидкого топлива и др. Успехи органической химии позволили рационально использовать нефть, каменный уголь, природный газ, лесохимическое и другое сырье. Пользуясь методами органической химии, удалось установить структуру белков, нуклеиновых кислот и других сложных природных соединений, синтезировать витамины, некоторые гормоны, ферменты. Ряд направлений органической химии благодаря их интенсивному развитию вырос в большие специальные разделы, напр. химия высокомолекулярных соединений.
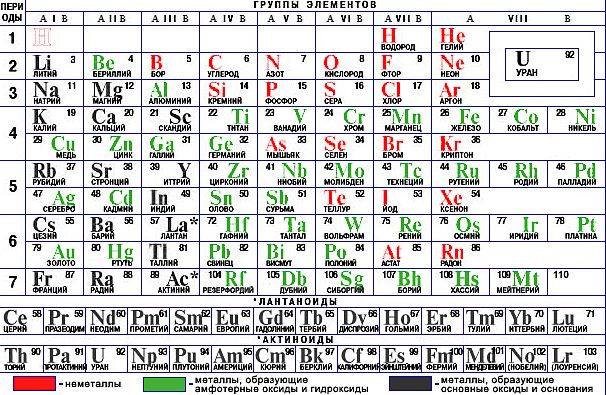
НЕОРГАНИЧЕСКАЯ ХИМИЯ, изучает химические элементы и образуемые ими простые и сложные вещества (кроме органических соединений углерода, которые изучаются органической химией). История развития неорганической химии тесно связана с общей историей химии (результатом изучения неорганических веществ явились важнейшие достижения химии кон. 18 — нач. 19 вв., напр. создание кислородной теории горения, открытие законов стехиометрии). Теоретические основы неорганической химии — периодический закон и периодическая система элементов Менделеева. Современная неорганическая химия изучает строение и свойства неорганических веществ с использованием не только химических, но и физических методов (напр., спектроскопии). Неорганическая химия — научная база основной химической промышленности (производство солей, кислот, щелочей) и металлургии. Число неорганических веществ составляет десятки тысяч. Достижения неорганической химии обеспечивают создание материалов новейшей техники — сверхчистых металлов, сплавов, пьезоэлектриков, полупроводников, сверхпроводников, облегченных стройматериалов, окислителей и горючего для космических ракет.
НЕОРГАНИЧЕСКАЯ ХИМИЯ, изучает химические элементы и образуемые ими простые и сложные вещества (кроме органических соединений углерода, которые изучаются органической химией). История развития неорганической химии тесно связана с общей историей химии (результатом изучения неорганических веществ явились важнейшие достижения химии кон. 18 — нач. 19 вв., напр. создание кислородной теории горения, открытие законов стехиометрии). Теоретические основы неорганической химии — периодический закон и периодическая система элементов Менделеева. Современная неорганическая химия изучает строение и свойства неорганических веществ с использованием не только химических, но и физических методов (напр., спектроскопии). Неорганическая химия — научная база основной химической промышленности (производство солей, кислот, щелочей) и металлургии. Число неорганических веществ составляет десятки тысяч. Достижения неорганической химии обеспечивают создание материалов новейшей техники — сверхчистых металлов, сплавов, пьезоэлектриков, полупроводников, сверхпроводников, облегченных стройматериалов, окислителей и горючего для космических ракет.

 Углеводороды
Углеводороды

 Предельные углеводороды (алканы или парафины)
Предельные углеводороды (алканы или парафины)
НАСЫЩЕННЫЕ СОЕДИНЕНИЯ (предельные соединения), органические соединения, в молекулах которых атомы соединены между собой только простыми связями в «открытые» цепи (алифатические насыщенные соединения) или циклы (алициклические насыщенные соединения). К насыщенным соединениям относятся, напр., алканы, или парафины, общей формулы СnH2n+2 (метан СН4, этан С2Н6), циклоалканы, или циклопарафины, СnH2n (циклопропан С3Н6, циклогексан С6Н12). Насыщенные углеводороды содержатся главным образом в нефти и природном газе. Их производные получают различными синтетическими методами.
ПАРАФИН, воскоподобное вещество, смесь предельных углеводородов состава С18Н38—С35Н72. tпл 40-65 °С; плотность 0,880-0,915 г/см3 (15 °С). Получают главным образом из нефти. Применяют для приготовления парафинистой бумаги, пропитки древесины в спичечном и карандашном производствах, для аппретирования тканей, как изоляционный материал, химическое сырье и т. д. В медицине используется для парафинолечения.
ПАРАФИН, воскоподобное вещество, смесь предельных углеводородов состава С18Н38—С35Н72. tпл 40-65 °С; плотность 0,880-0,915 г/см3 (15 °С). Получают главным образом из нефти. Применяют для приготовления парафинистой бумаги, пропитки древесины в спичечном и карандашном производствах, для аппретирования тканей, как изоляционный материал, химическое сырье и т. д. В медицине используется для парафинолечения.
 Непредельные углеводороды (алкены, алкадиены и алкины)
Непредельные углеводороды (алкены, алкадиены и алкины)
НЕНАСЫЩЕННЫЕ СОЕДИНЕНИЯ (непредельные соединения), органические соединения, в молекулах которых атомы соединены между собой кратными (двойными, напр. С=С; тройными, напр. СєС) связями в «открытые» цепи (алифатические ненасыщенные соединения) или циклы (алициклические ненасыщенные соединения и ароматические). К ненасыщенным соединениям относятся, напр., олефины, диены, ацетилен, циклогексен, бензол. Ненасыщенные соединения характеризуются высокой реакционной способностью.
ОЛЕФИНЫ (алкены), ненасыщенные ациклические углеводороды, содержащие в молекуле одну двойную связь C=C. Первый член ряда олефинов — этилен CH2=CH2, поэтому олефины называются также этиленовыми углеводородами. Содержатся в продуктах переработки нефти и природных газов. Широко используются для синтеза полимеров и др. ценных промышленных продуктов.
ОЛЕФИНЫ (алкены), ненасыщенные ациклические углеводороды, содержащие в молекуле одну двойную связь C=C. Первый член ряда олефинов — этилен CH2=CH2, поэтому олефины называются также этиленовыми углеводородами. Содержатся в продуктах переработки нефти и природных газов. Широко используются для синтеза полимеров и др. ценных промышленных продуктов.
 Ароматические углеводороды (арены)
Ароматические углеводороды (арены)
АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ, органические соединения, молекулы которых содержат циклы (т. н. бензольные ядра) из 6 атомов углерода, участвующих в образовании единой системы сопряженных связей. Включают углеводороды (арены) и их производные (анилин, бензойная кислота, фенол и др.). К ароматическим соединениям относят также т. н. небензоидные соединения, напр. азулен, гетероциклические соединения — фуран, тиофен, пиридин и др. Название связано с тем, что первые открытые представители ароматических соединений обладали приятным запахом. Основные источники ароматических соединений — продукты нефтепереработки и каменноугольная смола.
АРЕНЫ, ароматические углеводороды, содержащие одно или несколько бензольных колец (в т. ч. конденсированных). Примеры — бензол, толуол, нафталин, антрацен, фенантрен.
АРЕНЫ, ароматические углеводороды, содержащие одно или несколько бензольных колец (в т. ч. конденсированных). Примеры — бензол, толуол, нафталин, антрацен, фенантрен.
 Органические соединения
Органические соединения

 Белки
Белки
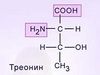
БЕЛКИ, высокомолекулярные органические соединения, биополимеры, построенные из 20 видов L-a-аминокислотных остатков, соединенных в определенной последовательности в длинные цепи. Молекулярная масса белков варьируется от 5 тыс. до 1 млн. Название «белки» впервые было дано веществу птичьих яиц, свертывающемуся при нагревании в белую нерастворимую массу. Позднее этот термин был распространен на другие вещества с подобными свойствами, выделенные из животных и растений. Белки преобладают над всеми другими присутствующими в живых организмах соединениями, составляя, как правило, более половины их сухого веса. Предполагается, что в природе существует несколько миллиардов индивидуальных белков (например, только в бактерии кишечной палочки присутствует более 3 тыс. различных белков). Белки играют ключевую роль в процессах жизнедеятельности любого организма. К числу белков относятся ферменты, при участии которых протекают все химические превращения в клетке (обмен веществ); они управляют действием генов; при их участии реализуется действие гормонов, осуществляется трансмембранный транспорт, в том числе генерация нервных импульсов. Они являются неотъемлемой частью иммунной системы (иммуноглобулины) и системы свертывания крови, составляют основу костной и соединительной ткани, участвуют в преобразовании и утилизации энергии и т. д.
 Жиры (липиды)
Жиры (липиды)
ЛИПИДЫ (от греч. lipos — жир), обширная группа природных органических соединений, включающая жиры и жироподобные вещества. Молекулы простых липидов состоят из спирта и жирных кислот, сложных — из спирта, высокомолекулярных жирных кислот и других компонентов. Содержатся во всех живых клетках. Липиды — один из основных компонентов биологических мембран. Образуют энергетический резерв организма, участвуют в передаче нервного импульса, в создании водоотталкивающих и термоизоляционных покровов и др. К липидам относят некоторые жирорастворимые вещества, в молекулы которых не входят жирные кислоты, напр., терпены, стерины. Многие липиды — продукты питания, используются в промышленности и медицине.
 Углеводы
Углеводы
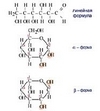
УГЛЕВОДЫ, обширная группа природных органических соединений, химическая структура которых часто отвечает общей формуле Cm(H2O)n(т. е. углерод вода, отсюда название). Различают моно-, олиго- и полисахариды, а также сложные углеводы — гликопротеиды, гликолипиды, гликозиды и др. Углеводы — первичные продукты фотосинтеза и основные исходные продукты биосинтеза других веществ в растениях. Составляют существенную часть пищевого рациона человека и многих животных. Подвергаясь окислительным превращениям, обеспечивают все живые клетки энергией (глюкоза и ее запасные формы — крахмал, гликоген). Входят в состав клеточных оболочек и других структур, участвуют в защитных реакциях организма (иммунитет). Применяются в пищевой (глюкоза, крахмал, пектиновые вещества), текстильной и бумажной (целлюлоза), микробиологической (получение спиртов, кислот и других веществ сбраживанием углеводов) и других отраслях промышленности. Используются в медицине (гепарин, сердечные гликозиды, некоторые антибиотики).
 Нуклеиновые кислоты
Нуклеиновые кислоты
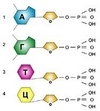
НУКЛЕИНОВЫЕ КИСЛОТЫ (полинуклеотиды), высокомолекулярные органические соединения, обеспечивающие хранение и передачу наследственной (генетической) информации в живых организмах из поколения в поколение. В зависимости от того, какой углевод входит в состав нуклеиновой кислоты — дезоксирибоза или рибоза, различают дезоксирибонуклеиновую (ДНК) и рибонуклеиновую (РНК) кислоты. Последовательность нуклеотидов в нуклеиновых кислотах определяет их первичную структуру.




